D Blok Elemanları ve Geçiş Elemanları Arasındaki Fark | D Blok Elemanları vs Geçiş Elemanları
Anahtar Farkı - D Blok Elementleri ve Geçiş Elementleri
D-Blok elemanları ve geçiş arasındaki fark elementler oldukça kafa karıştırıcıdır. Her iki kelime birbirlerinin yerine kullanılır ve birçok kişi d-blok elemanları için 'geçiş elementleri' kelimesini kullanır. D-blok elemanları ve geçiş elementleri arasındaki anahtar farkı tüm geçiş elementleri D-blok elementleri , ise tüm D-bloğu elemanları geçiş elemanları değildir . D-blok elemanlarının d-alt kabuğunda d elektronlarına sahip olduğu açıktır. Geçiş unsurları, tam olarak d doldurulmuş kalıcı iyonlar oluşturan elementlerdir. Örneğin Çinko ve Scandium, d-blok elemanlarıdır; geçiş elementleri değil.
D-blok Elemanları Nedir? D blok elemanları elektron konfigürasyonu ve periyodik tablonun konumu kullanılarak açıkça tanımlanabilir. D-blok elemanın asıl özelliği

alt kabuğunda en az bir elektrona sahip olmasıdır. Tek şey, d-blok elementlerdeki elektronların Aufbau prensiplerine göre doldurulması 4s -elektronlar önce 3d -elektronlar önce doldurulur; yani 3d-elctronların 4s-elektronlardan daha yüksek enerjiye sahip olduğu anlamına gelir. Ancak, iyonlar oluşturmak için elektronları çıkardıklarında; 4s - Elektronlar önce atomdan çıkarılır.
| Elektron Konfigürasyonu | Scandium | |
| Sc | [Ar] 3d | 1 4s 2 Titanyumdan Önce Orta |
| [Ar] 3d | 3 4s 2 2 | |
| 2 | V | [Ar] 3d 5 |
| 4s | Krom Cr [Ar] 3d 5 | |
| 4s | 2 Demir Fe [Ar] 3d | |
| 6 | 4s | 2 Kobalt Co [Ar] 3d |
| 7 | 4s | 2 Bakır Cu [Ar] 3d |
| 4s | 2 Nikel Ni | |
| 10 | 4s | 1 Çinko Zn [Ar] 3d |
| 10 | 4s | 2 -> -> Not: [Ar] = 1s |
2s 2 2p 6 3s 2 3p 6 Geçiş Elemanları Nedir? Geçiş elemanları, tam doldurulmamış d-orbitalleri ile kararlı iyonlar oluşturan elementlerdir. İyonlar d blok elemanlarla oluşturulduğunda; önce s
-elektronları (n-düzeyi) ortadan kaldırır ve daha sonra
d -elektronları (n-1 düzeyi) kaldırırlar. Çinko ve Scandium, d-blokta iki özel elementtir; tam olarak d doldurulmuş olmayan iyonlar oluşturmazlar; bu nedenle geçiş öğeleri olarak düşünülmez.D-grubundaki diğer elementlerin tamamı, d elektronlarını eksik dolduran kararlı iyonlar oluşturmaktadır. Geçiş Metal Çözümleri D-blok Elemanları ve Geçiş Elemanları arasındaki fark nedir? D-Blok Elemanlarının Tanımı ve Geçiş Elemanları

D-Blok Elemanları:
d-
alt kabuğunda bir veya daha fazla d- elektronu bulunan elementler d-blok elemanları olarak bilinirler. D-blok elementlerin çoğu metallerdir. Geçiş Elemanları: Eksik olarak doldurulmuş d
aralıklı sabit iyonlar oluşturabilen elementlere geçiş elementleri denir. Not: Zn ve Sc geçiş elementleri değildir. Doldurulmamış d-orbitalleri içermeyen sadece Zn 2+
ve Sc
3+ iyonlarını oluşturmazlar. Zn 2 + = 1 s
2 2s 2 2 p 6 3 S 2 3p 6 3 boyutlu 10 Sc 3+ = 1 s
2 2s 2 2 p 6 3 S 2 3p 6 3d 10 Aşağıdaki iyonlar doldurulmamış d-orbitalleri içerir. Dolayısıyla bu elementler geçiş elementi olarak kabul edilir. Cu 2+
= 1s
2 2s 2 6 3s 2 3p 6 3d 9 Ni 4+ = 1s 2
2s 2 2p 6 3s 2 2 2 2 6 3 6 3d 6
Mn 2+ = 1s 2 2s 3s 2 3 6 3d 5 Fe 2+
= 1s 2 2s 2 Oksidasyon Durumları: D-Blok Elemanları: 2p 6 3s 2 3p 6 3d
D-blok elemanları çoklu oksidasyon durumlarını göstermektedir ve bunların azı tek bir oksidasyon halini göstermektedir.
Örnek: Çinko sadece +2 oksidasyon durumunu gösterir ve Scandium sadece +3 oksidasyon durumunu gösterir.
D-bloğundaki diğer elementler çoklu oksidasyon durumlarını gösterir.
Geçiş Elemanları:
Geçiş öğeleri, çoklu oksidasyon durumları gösterir. En az bir devlet doldurulmamış
d - boşluklar içeriyor. Örnek: Titanyum +2, +4
Vanadyum +2, +3, +4, +5
Krom +2, +3, +6
Manganez +2, +3, +4, +6, +7
Demir +2, +3
Kobalt +2, +3
Nikel +2, +4
Bakır +1, +2
Resim Nezaket:
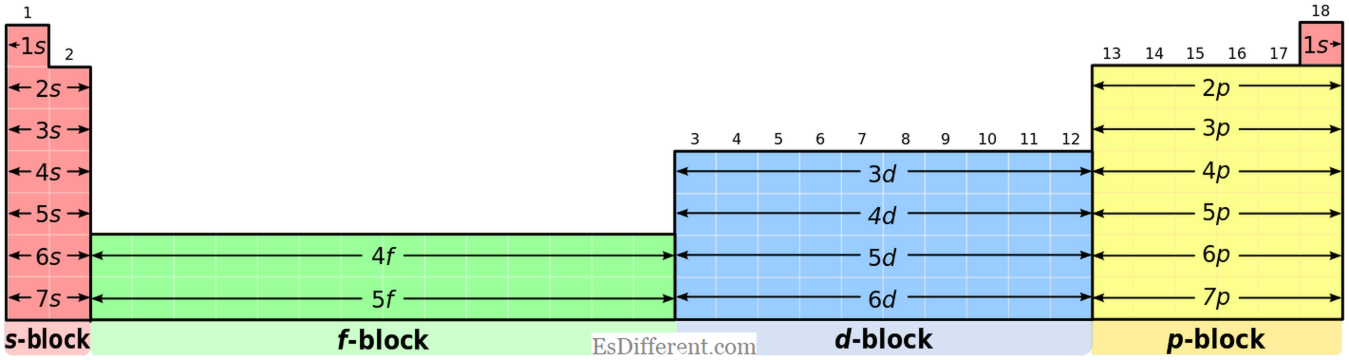
1. "Periyodik tablo blokları spdf (32 sütun)" kullanıcısı tarafından: DePiep [CC BY-SA 3. 0] via Commons
2. "Renkli geçiş metali çözümleri" [Public Domain] Commons aracılığıyla




