Metan ve Etan Arasındaki Fark | Metan vs Etan
Anahtar Difference - Methane vs Ethane
Methane ve Ethane, alkan ailesinin en küçük üyesidir. Bu iki organik bileşiğin moleküler formülleri, sırasıyla CH 4 ve C 2 H 6 dır. Metan ve Etan arasındaki anahtar fark , bunların kimyasal yapıdadır; Bir etan molekülü, metil gruplarının dimer olarak birleştirilen iki metil grubu olarak düşünülür. Diğer kimyasal ve fiziksel farklılıklar ağırlıklı olarak bu yapısal farklılıktan kaynaklanmaktadır.
Metan Nedir?
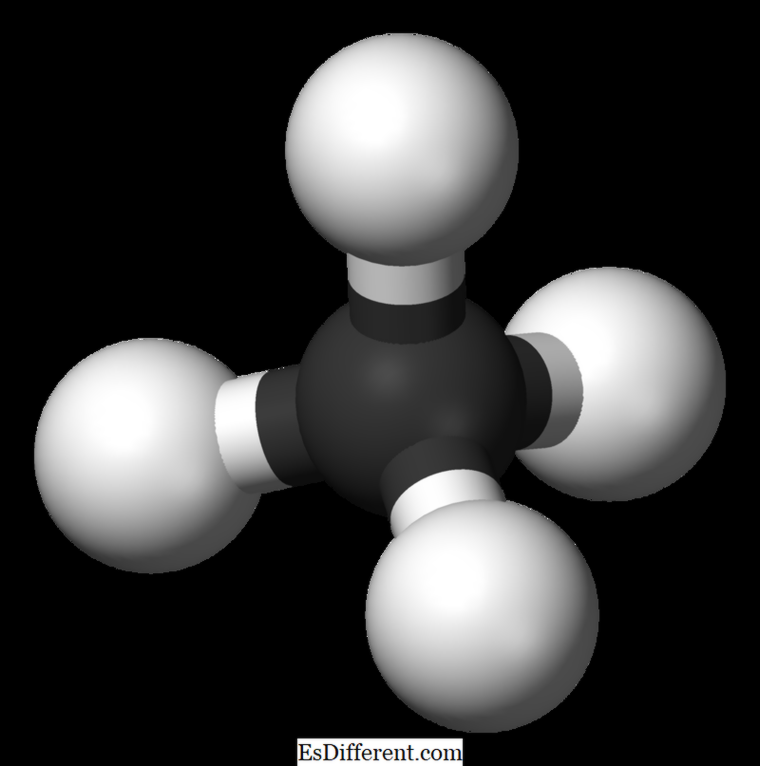
Metan, CH 4 (dört hidrojen atomu bir karbon atomuna bağlı) ile alkan ailesinin en küçük üyesidir. Doğalgazın ana bileşeni olarak kabul edilir. Metan renksiz, kokusuz ve tatsız bir gazdır; karban, bataklık gazı, doğal gaz, karbon tetrahidrid, ve hidrojen karbür olarak da bilinir. Kolaylıkla ateşlenebilir ve buhar havadan daha açıktır.
Metan doğal olarak yer altında ve deniz tabanı altında bulunur. Atmosfer metan bir sera gazı olarak kabul edilir. Metan atmosferde su ile CH 3 'e ayrılır.
Ethane nedir?
Etilen, standart sıcaklık ve basınçta renksiz, kokusuz, gaz halindeki bileşiktir. Moleküler formülü ve molekül ağırlığı sırasıyla C 2 H 6 ve 30. 07 g.mol -1 'dır. Petrol rafine etme işleminden gelen yan ürün olarak doğal gazdan izole edilmiştir. Etilen üretimi etan çok önemlidir.

Metan ve Etan arasındaki fark nedir?
Metan ve Etanın Özellikleri
Metan:
Metan moleküler formülü CH 4, ve bu bir örnektir dört eşdeğer CH bağı olan bir tetrahedral molekülün (sigma bağları). H-C-H atomları arasındaki bağ açısı 109.5 0 ve tüm C-H bağları eşdeğerdir ve 108'ye eşittir. Saat 70. Etilen:

Etilen 'un moleküler formülü 2 H 6, ve doymuş bir hidrokarbon. Çünkü çoklu bağlar içeriyor. Kimyasal Özellikler: Metan: Kararlılık:

Metan, KMnO
4
, K 2 Cr < 2 0 7 , H 2 4 veya HNO 3 . Yakma: Metan, fazla hava veya oksijen varlığında soluk mavi parlak olmayan bir alevle yanar ve karbon dioksit ve su üretir.Oldukça ekzotermik bir reaksiyon; Bu nedenle, mükemmel bir yakıt olarak kullanılır. Yetersiz hava veya oksijen varlığında kısmen karbon monoksit (CO) gazı yanar. Yerine Getirme Reaksiyonları: Metan halojenlerle ikame reaksiyonları gösterir. Bu reaksiyonlarda, bir veya daha fazla hidrojen atomu, eşit miktarda halojen atomuyla değiştirilir ve buna "halojenasyon" denir. "Güneş ışığı altında klor (Cl) ve brom (Br) ile tepki verir. Buharla Reaksiyon:
Metan ve buhar karışımı, alüminyum yüzey üzerinde ısıtılan (1000 K) nikel ile taşınırsa, hidrojen üretebilir. Piroliz:
Metan yaklaşık 1300 ° C'ye ısıtıldığında karbon karası ve hidrojene ayrışır. Etan:
Reaksiyonlar: Etilen gaz (CH 999 3 999 3 999) bromoetan oluşturmak için bromin buharı ile reaksiyona girerek (CH Br) ve hidrojen bromür (HBr) gibi bir baz varlığında reaksiyona girer. Bu bir ikame reaksiyonudur; etan içindeki bir hidrojen atomu bromin atomuyla ikame edilir. CH
3 3
3
+ Br 2 CH 3 CH 2 Br + HBr Yanma: Etanın tamamen yanması 1559.7 kJ / mol (51.9 kJ / g) ısı, karbon dioksit ve su üretir. 2 2
2 H 6 +7 O 2 → 4 CO 2 + 6 H 2
O + 3120 kJ
Ayrıca oksijen fazlalığı olmadan ortaya çıkabilir ve amorf karbon ve karbon monoksit karışımı üretir. 2 C 2 H 6 + 3 O 2 → 4 C + 6 H 2 O + enerji 2 C 2
H
6 + 5 O 2 → 4 CO + 6 H 2 2 + 2 2 2 6
+ 4 0 2 + enerji Substitusyon Reaksiyonları: Yer değiştirme reaksiyonu, kimyasal bir bileşik içindeki bir fonksiyonel grubun yer değiştirmesini içeren bir kimyasal tepkimedir ve tarafından başka bir işlevsel grup değiştirdi. Kullanım Alanları: Metan:
Metan pek çok endüstriyel kimyasal işlemlerde (bir yakıt, doğal gaz, sıvılaştırılmış doğal gaz gibi) kullanılır ve soğutulmuş bir sıvı olarak taşınır. Etan: Etanlar, motorlar için bir yakıt ve aşırı derecede düşük sıcaklıklı bir sistem için bir soğutucu olarak kullanılır. Çelik silindirlere kendi buhar basıncı altında sıvılaştırılmış bir gaz olarak gönderilir. Kaynaklar: "Ethane". Vikipedi . N. s., 2016. Web. 7 Haziran 2016. Khanna, Bhishm. "Metanın Kimyasal Özellikleri Nedir? ”. Preservearticles. com . N. s., 2016. Web. 7 Haziran 2016. "Metan | CH4 - Pubchem ". pubchem. NCBI. nlm. NIH. gov . N. s., 2016. Web. 7 Haziran 2016. "Metan". Vikipedi . N. s., 2016. Web. 7 Haziran 2016 Image Nezaket: Commons vasıtasıyla (Kamusal Alan) tarafından "Metan molekülünün bilye ve çubuk modeli" Wikimedia "Benekli etan molekülünün bilye ve çubuk modeli" Ben Ben Mills - Ortak Çalışma (Public Domain) via Commons Wikimedia "Methane" Jynto - Dosyaya dayalı kendi eser: Methane-CRC-MW-dimensions-2D.png, (Kamusal Alan) Commons Wikimedia "Ethane" (Kamu Alanı) via Commons Wikimedia


