Lizin ve L-lisin Arasındaki Fark | Lizin ile L-lizin
Anahtar Farkı - Lizin-L-lizin
Lizin ve L-lisin her ikisi de aynı fiziksel özellikleri paylaşan amino asitler türüdür, aralarındaki bazı farklar. Lizin ve L-lisin arasındaki anahtar fark, düzlem polarize ışığı döndürme kabiliyetindedir. Lizin biyolojik açıdan aktif doğal bir α-amino asididir. Şiral karbon atomu etrafında iki farklı enantiyomer oluşturulması ihtimalinden dolayı iki izomerik formda ortaya çıkabilir. Bunlar solak ve sağ el konfigürasyonlarına benzer şekilde L ve D formları olarak bilinirler. Bu L- ve D-formlarının optik olarak aktif oldukları ve düzlem polarize ışığı farklı bir anlamda döndürdüğü söylenir; saat yönünde veya saatin aksi yönde Işık lizini saat yönünün tersine döndürürse ışık düz bir levha gösterir ve L-lisin olarak bilinir. Bununla birlikte, burada izomerlerin D- ve L- etiketlemelerinin d- ve l-etiketi ile aynı olmadığına dikkat edilmelidir.
Lizin Nedir?
Lizin, esansiyel amino asit olup, vücudumuzda sentezlenmemiştir ve düzenli diyetle tedarik edilmelidir. Bu nedenle lizin, insanlar için önemli bir amino asittir. Kimyasal formül NH 2 - (CH 2) olan amin (-NH 2 ) ve karboksilik asit (-COOH) işlevsel gruplarından oluşan biyolojik olarak önemli bir organik bileşiktir >) ' 4 , -CH (NH 2 ) - -COOH. Lizin'in temel unsurları karbon, hidrojen, oksijen ve azottur. Biyokimyada hem amin hem de karboksilik asit grupları ilk (alfa-) karbon atomuna bağlı olan amino asitler a-amino asitler olarak bilinir. Böylece lisin, aynı zamanda α-amino asitler olarak da düşünülür. Lizin yapısı Şekil l'de verilmiştir. Şekil 2: Lizin moleküler yapısı (* karbon atomu bir şiral veya asimetrik karbon atomudur ve aynı zamanda alfa-karbon atomunu temsil eder) Lizin doğada basittir çünkü iki bazik amino içerir grupları ve bir asidik karboksilik asit grubu. Bu nedenle, iki amino grubunun varlığı nedeniyle geniş hidrojen bağını oluşturmaktadır.
İyi lizin kaynakları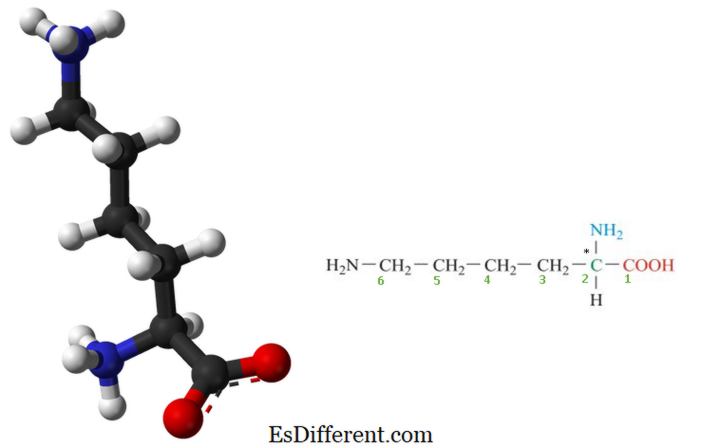
yumurta, kırmızı et, kuzu, domuz eti ve kümes hayvanları, peynir ve bazı balıklar (örn. Morina ve sardalya gibi) gibi protein açısından zengin hayvansal kaynaklardır. Lizin ayrıca
bitki proteinleri bakımından zengin, soya, bakla ve bezelye gibi. Bununla birlikte, çoğu hububat tanesinde sınırlayıcı bir amino asittir ancak çoğu puls ve baklagillerde bol miktarda bulunur.
'dır.Ayrıca lisin, asimetrik veya kiral karbon atomunun varlığına bağlı olarak optik olarak aktif bir amino asittir. Böylece, lisin, aynı molekül formülüne sahip olan izomerik moleküller olan ancak uzaydaki atomlarının üç boyutlu oryantasyonlarında farklı olan stereoizomerleri yaratabilir. Enantiomerler, bir yansıma ile birbiriyle ilişkili olan iki stereoizomerdir veya üst üste binemeyen birbirlerinin ayn görüntülerdir. Lizin, L- ve D- olarak bilinen iki enantiyomerik formda bulunur ve lisin enantiyomerleri şekil 2'de verilmektedir. Şekil 2: Lisin amino asidin enantiomerleri. COOH, H, R ve NH2 grupları, C atomunun etrafında saat yönünde düzenlenir, enantiomerin adı L-form ve D-formudur. L- ve D- sadece karbon atomu etrafındaki mekansal düzenlemeye atıf yapar ve optik aktiviteye göndermezler. Şiral bir molekülün L- ve D-formları farklı yönde polarize ışığın düzlemini döndürürken, bazı L-formları (veya D-formları) ışığı sola (levo veya l-form) döndürür ve bazıları sağa döndürür (dekstro veya d-form). l- ve d-formlarına optik izomerler denir. L-lisin ve D-lisin polarize ışığı döndürdükleri yön hariç, birbirlerinin aynı fiziksel özelliklerine sahip enantiyomerlerdir. Süperleştirilemez ayna görüntüsü ilişkisine sahiptirler. Bununla birlikte, D ve L'nin terminolojisi, lisin dahil amino asitlerinde yaygın değildir. Düzlem polarize ışığı aynı büyüklükte ama farklı yönlerde döndürürler. Düzlem polarize ışığı saat yönünde döndüren lisin D ve L-izomerine, kutup açıcı veya
d-lizin adı verilir ve düzlem polarize ışığı saatin ters yönünde döndüren loşin okorometrik veya L-lisin (Şekil 2). L-Lizin,

'un en güvenilir kararlı lisin şekli
' tür. D-Lizin sentetik bir lizin formudur ve l-lisinden rasemizasyon yoluyla sentezlenebilir. Bu, hücre bağını güçlendirmek için bir kaplama malzemesi olarak kullanılan poli-d-lisinin işlenmesinde kullanılır. L-Lizin, insan vücudunda, kalsiyum emiliminde, kas protein gelişiminde ve hormonların, enzimlerin ve antikorların sentezinde önemli bir rol oynamaktadır. Endüstriyel olarak, L-lisin, Corynebacterium glutamicum kullanan bir mikrobik fermantasyon işlemi ile üretilir. Lizin ve L-lisin arasındaki fark nedir? Lizin ve L-lisin, polarize ışığı döndürdükleri yön hariç, aynı fiziksel özelliklere sahiptir. Sonuç olarak, L-lisin, önemli ölçüde farklı biyolojik etkilere ve işlevsel özelliklere sahip olabilir. Bununla birlikte, bu biyolojik etkileri ve fonksiyonel özellikleri ayırt etmek için çok sınırlı araştırma yapılmıştır. Bu farklılıklardan bazıları şunları içerebilir:
Taste L-lizin: L-amino asitler, tatsız olma eğilimindedir. D-lizin: D-amino asit formları tatlı olma eğilimindedir.
Bu nedenle, l-lizin, lizinden daha az / daha tatlı olabilir.
Bolluk
L-lizin:
l-lizin de dahil olmak üzere amino asitin l-formları doğada en bol formdur.Bir örnek olarak, proteinlerde yaygın olarak bulunan ondokuz L-amino asitten dokuzu sağa dönüktür ve geriye kalan levonotatiftir. D-lizin:
Deneysel olarak gözlenen amino asitlerin D-formlarının çok nadir görülmesi bulundu. Kaynaklar: Solomons, T.W. Graham ve Graig B. Fryhle (2004). Organic Chemistry (8 999 inci
ed). Hoboken: John Wiley & Sons, Inc. Everhardus, A. (1984). Stereokimya, farmakokinetiği ve klinik farmakolojide sofistike saçmalıkların temelini oluşturan
Avrupa Klinik Farmakolojisi Dergisi,
26 , 663-668. Image Nezaket: Ben Mills'in "L-lizin-monoksite-hidroklorür-dihidrat-xtal-3D-topları" - Wikimedia Commons aracılığıyla kendi çalışmaları




