Sigma ve Pi bağ arasındaki fark
Sigma Bağları Nedir?
Sigma bağları, atomların bağlı çekirdeğini birbirine bağlayan eksen boyunca oluşturulan moleküller içindeki atomlar arasındaki bağlardır.
Moleküler bağlar
Moleküller, atomlar kimyasal bağlar vasıtasıyla elektronları değiştirirken veya paylaştıklarında oluşur. Aslında üç tür tahvil var. İyonik bağlar, metalik bağlar ve kovalent bağlar. İyonik bağlarda, atomlar bir elektron değiştirecek, böylece bir atom pozitif yüklü olacak ve diğeri negatif yüklenecek, böylece elektromanyetik kuvvete çekilecektir. Metalik bağlarda, elektronlar, molekülün tamamı boyunca eşit olarak dağıtılacak, elektronları çeken pozitif yüklü iyonları saran serbest, delokalize edilmiş bir elektron denizi yaratacak.
Kovalent bağlar içinde elektronlar paylaşılır ve paylaşım şekli, elektronların olasılık bulutları ve bulundukları orbitaller aracılığıyla, kabaca simetrik olacak şekilde örtüşür.
Orbitaller ve sigma bağı
Orbitaller belirli enerji seviyeleri ile ilişkili atomların etrafındaki bölgelerdir. Çekirdekten uzakta bulunan orbitallerdeki elektronlar çekirdeğe daha yakın orbitallerdeki elektronlardan daha fazla enerjiye sahip olacaklar. Bir atomun orbitalleri, başka atomlardan gelen orbitallerle çakıştığında moleküler bağlar oluşturan moleküler orbitaller oluşturur; bu da moleküller için elbette ki izin verir.
Sigma bağları, atomlar arasında oluşacak ilk bağ türüdür. Bir sigma bağında, elektron olasılığı bulutları, bağlı atomların çekirdeklerini birleştiren eksende olacak. Farklı atomlardan gelen s orbitalleri bir bağ oluşturulması için çakıştığında, genellikle sigma bağları oluşur. yörüngesi, çekirdeğin etrafında bir küre gibi düzenlendiğinden, her iki çekirdek arasında eksen boyunca oluşacaktır.
Sigma bağları ve sigma orbitalleri
Sigma bağını oluşturan elektronlar sigma orbitalleri içinde olacak ve dolayısıyla bağlı atomların çekirdeklerini birbirine bağlayan eksen boyunca bir yerde olacaktır. Bununla birlikte, sigma bağları, elektronların bir sigma bağlayıcı orbitalinde mi yoksa bir anti-bağlama yörüngesinde mi olduğuna bağlı olarak kararlı veya kararsız olabilir.
Sigma bağlanma orbitalleri çekirdeklerin arasındaki boşlukta bulunurken, anti-bağlayıcı orbitaller çekirdeği birbirine bağlayan eksende olacak, ancak atomların iki tarafı arasındaki boşluğun karşısında olacak. Daha fazla elektron bağlanma yörüngelerinde ve daha fazla anti-bağlayıcı orbitallerde veya her ikisinde de eşit miktarda elektron var ise dengesiz olduğunda, sigma bağ dengede olacaktır.
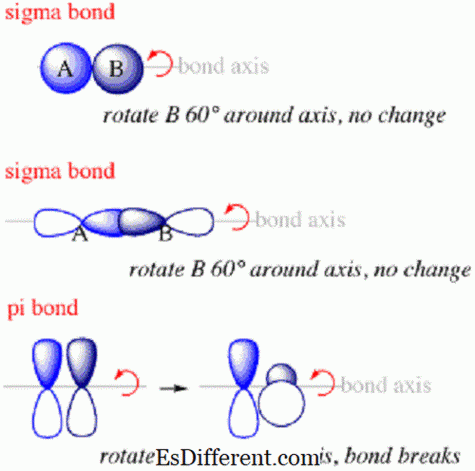
Pi bağı nedir?
Pi bağları, elektronların, eklem boyunca değil, birleştirilmiş atomların çekirdeklerini birleştiren eksenin üstünde ve altında olduğu moleküllerdeki atomlar arasındaki bağlardır.Bunlar, sigma bağından sonra bir molekül içinde oluşacak ikinci tür bağlardır.
Pi bağları ve p orbitalleri
Pi bağlarının bağlanma ekseninin üstünde ve altında oluştuğu ancak bununla birlikte olmadığı nedeni, genellikle p gibi örtüşen orbitallerden oluşmasıdır, bağlı atomlar üzerindeki orbitaller. Bu orbitallerin çekirdeğinde bir elektron yoğunluğu yoktur. Sonuç olarak, örtüşen p orbitallerinden oluşan pi bağlarını oluşturan elektronlar, çekirdeğe doğrudan bitişik olmayan bir bölgede daima kümelenir. Pi bağları, p orbitalleriyle ortak özelliklere sahip olan d orbitalleri gibi diğer atomik orbitaller arasında da oluşabilir.
Pi bağları ve pi orbitalleri
Farklı atomların p orbitalleri çakıştığında pi bağlarının oluşmasına izin veren moleküler pi orbitalleri oluştururlar. Bağ, elektronun bulunduğu yörüngeye bağlı olarak bir kez daha kararlı ya da kararsız olabilir. Pi bağlanma orbitallerinde daha fazla elektron varsa, pi bağları kararlı olacaktır. Anti bağlanma orbitallerinde daha fazla varsa ya da her ikisinde de eşit sayıda varsa kararsız olacaktır.
Sigma bağları ve pi bağları arasındaki benzerlikler
Sigma bağları ve pi bağları, her ikisi de belirli atomik orbitallerin üst üste gelmesinden türetilen spesifik molekül orbitallerine dayanır, örneğin durumda s orbitalleri pi ba¤lar> nda p orbitallerinden olufluyordu. Ayrıca, elektronların bağ molekül orbitallerinde veya anti-bağlayıcı moleküler orbitallerde olup olmamasına bağlı olarak kararlı veya kararsız olabilirler.
Sigma bağı ve pi bağı arasındaki farklar
Benzerliklerine rağmen önemli farklılıklar vardır.
- Sigma bağlarını oluşturan elektronlar, birleşmiş çekirdekleri birleştiren eksende uzayda dağıtılırken, pi bağlarındaki elektronlar eksenin üstünde ve altında dağılır ancak bununla birlikte dağılmaz.
- Sigma bağları, moleküller içindeki atomlar arasında oluşacak ilk bağlardır; pi bağları ikincidir.
- Sigma bağları sıklıkla farklı atomlarda s orbitallerinin kombinasyonu ile oluşurken, pi bağları p kombinasyonundan ve farklı atomlarda benzer orbitallerden oluşur.
- Buna ek olarak, pi bağları oluşturan örtüşen orbitallerin yönelimi, sigma bağları oluşturan üst üste binen orbitallerle orantılı olacaktır.
Sigma bağları vs. pi bağları
| Sigma bağı | Pi bağ |
| Atomik orbitaller, birleştirme ekseni | boyunca örtüşürler. Atomik orbitaller, birleştirme ekseni üstünde ve altında |
| İlk moleküller içindeki atomlar arasında bağ oluşturur | |
| orbitalleri gibi çakışan orbitallerden oluşan | p orbitalleri gibi örtüşen orbitallerden oluşan moleküller içindeki atomlar arasında ikinci bağlar örtüşen orbitaller |
| Sigma bağlarına dik olan orbitaller | Özet: Sigma ve Pi Bağları |
Sigma bağı, bir molekül içindeki atomlar arasındaki bağdır ve genellikle
s < eklem boyunca birleşmiş çekirdekleri birbirine örterek orbitaller.Oluşturulan ilk şey budur ve kararlılığı, elektronların sigma yapışkanlı ve anti-bağlayıcı orbitallerde nasıl dağıldığına bağlıdır. Pi bağları, farklı atomlardan gelen p orbitalleri ile örtüşen moleküler bağlardır. Pi bağlarını oluşturan elektronlar, bağlı atomların çekirdeklerini bağlayan eksenin üstünde ve altında dağılırlar, ancak eksen boyunca dağılmazlar. Bu bağların kararlılığı ayrıca pi orbitallerin bağlanmasına ve bağlanmasına bağlıdır. Sigma bağları, moleküller içinde oluşacak ilk bağlar olurken, pi bağları oluşacak ikinci bağ olacaktır. Pi bağları da, sigma bağlarını oluşturanlara dik olan atomik orbitallerden oluşur.




